基于小时候的自然课,大家对于大气污染,第一反应往往都是酸雨,但实际上,在对我们生活层面的影响上,光化学烟雾的危害远大于酸雨。
光化学烟雾(photo-chemical smog[1])是汽车、工厂等污染源排入大气的碳氢化合物(HC)和氮氧化物(NOx)等一次污染物在阳光(紫外光)作用下发生光化学反应生成二次污染物,参与光化学反应过程的一次污染物和二次污染物的混合物(其中有气体污染物,也有气溶胶)所形成的烟雾污染现象,是碳氢化合物在紫外线作用下生成的有害浅蓝色烟雾。

图源:视觉中国
NOx主要包括NO和NO2,你没看错,我第一次看见NOX的时候也以为别人在和我开玩笑..
光化学烟雾产生的主要有害物质是什么?
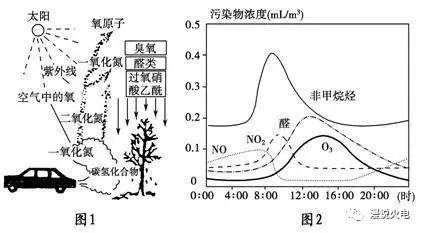
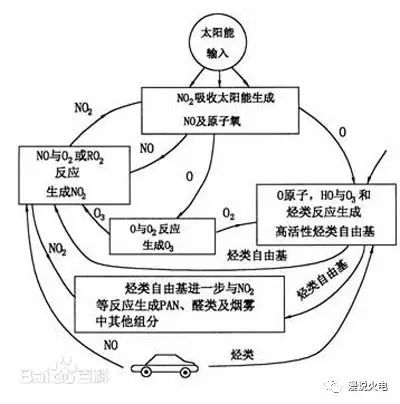
其实碰到化学,小编也是很脱力的。
化学式:
NO2==NO+O(条件为光照)
O+O2==O3
2NO+O2==2NO2
综合一下:
3O2==2O3(条件光照,NO2)

竟然生成了防止紫外线的臭氧!
臭氧是一种强氧化剂,在0.Ippm浓度时就具有特殊的臭味。并可达到呼吸系统的深层,刺激下气道黏膜,引起化学变化,其作用相当于放射线,使染色体异常,使红血球老化。PAN、甲醛、丙烯醛等产物对人和动物的眼睛、咽喉、鼻子等有刺激作用,其刺激域约为0.1ppm
光化学烟雾的重要一次性污染物是氮氧化物。来源是燃煤、燃油和汽车尾气。虽然燃煤排放氮氧化物总量超过汽车,但通常认为主凶是汽车尾气。原因是氮氧化物和氧气在阳光下产生臭氧的反应是可逆的,因此不能单独导致臭氧的高浓度。但是空气中的碳氢类活化分子,会加强这个产生臭氧的反应,因此易挥发有机化合物(VOC很多非甲烷烃就是),是光化学烟雾的重要组成部分。汽车因为其工作特点,经常处于不完全燃烧状态,同时排放大量HC,因此汽车尾气是光化学烟雾的主要贡献者。这是空气污染研究工作的里程碑之一,“洛杉矶烟雾”。
但是甩锅归甩锅,大量排放NOX这锅是怎么都甩不掉了。
为了祖国的环保事业,火电厂都做出了怎样的实际行动呢?
首先要从搞清楚这个NOx怎么来的?
一般认为在NOx中,一氧化氮约占90%以上,二氧化氮占5%~10%,产生的原因一般分为如下3种:
l 热力型NOx :高温下N2与O2反应生成的NOx
主要影响因素:温度、过量空气系数、在高温区的停留时间
在燃煤锅炉中,热力型NOx约占总排放量的10%~15%左右。
其实就是空气中的氮气和氧气在高温条件下反应了
l 燃料型NOx :燃料中的固定氮生成的NOx
这要说到煤的元素分析:全面测定煤种所含的全部化学成分叫做元素分析。煤中所含元素达到三十几种,一般将不可燃物质都归入灰分A,这样煤的元素分析包括;碳、氢、氧、氮、硫、灰分和水分,各化学元素成分用质量百分数表示,即。
C+H+O+N+S+A+M=100%
煤中的氧和氮是不可燃物质,但其含量也较少,煤炭中的氮含量一般在0.5%~2.5%左右。煤中的氮在高温条件下易生成污染大气的NOx,被视为有害元素。
在燃煤锅炉中,燃料型NOx占总排放量的比例为0%~85%
其实就是煤里的氮元素和氧元素反应了
l 快速型NOx :低温火焰下由于含碳自由基的存在生成的NOx
碳氢化合物燃料燃烧时,如果燃料浓度过浓,在反应区附近会快速生成NOx,燃料挥发物中碳氢化合物高温分解生成的CH自由基可以和空气中氮气反应生成HCN和N,再进一步与氧气作用以极快的速度生成NOx,所生成的NOx与炉膛压力的0.5次方成正比,与温度的关系不大
快速性NOx只在富氧情况下发生,其生成量一般占燃煤锅炉总NOx排放量的5%左右
其实就是科学家发现还有种特定情况也会生成NOx
屁话说了半天,就要控制以下几个条件,火焰温度、燃烧器区段氧浓度、燃烧产物在高温区停留时间和煤的特性。
然后落实到生产中我们能做到的有:降低火焰温度,防止局部高温;降低过量空气系数和氧浓度,使煤粉在缺氧的条件下燃烧。
这样我们就有了第一样法宝:低氮燃烧技术
具体的生产中的应用有
1 低过量空气燃烧
2空气分级燃烧
3 二次燃烧
4 浓淡偏差燃烧
5 低氮燃烧器技术
等等
这个根据每个锅炉技术参数不同而不同,我们就不具体展开分析了。实际上一旦燃烧器安装完成,运行人员只要知道燃烧调整原则即可以。
这样我们可以把排大气的NOx减小一大截
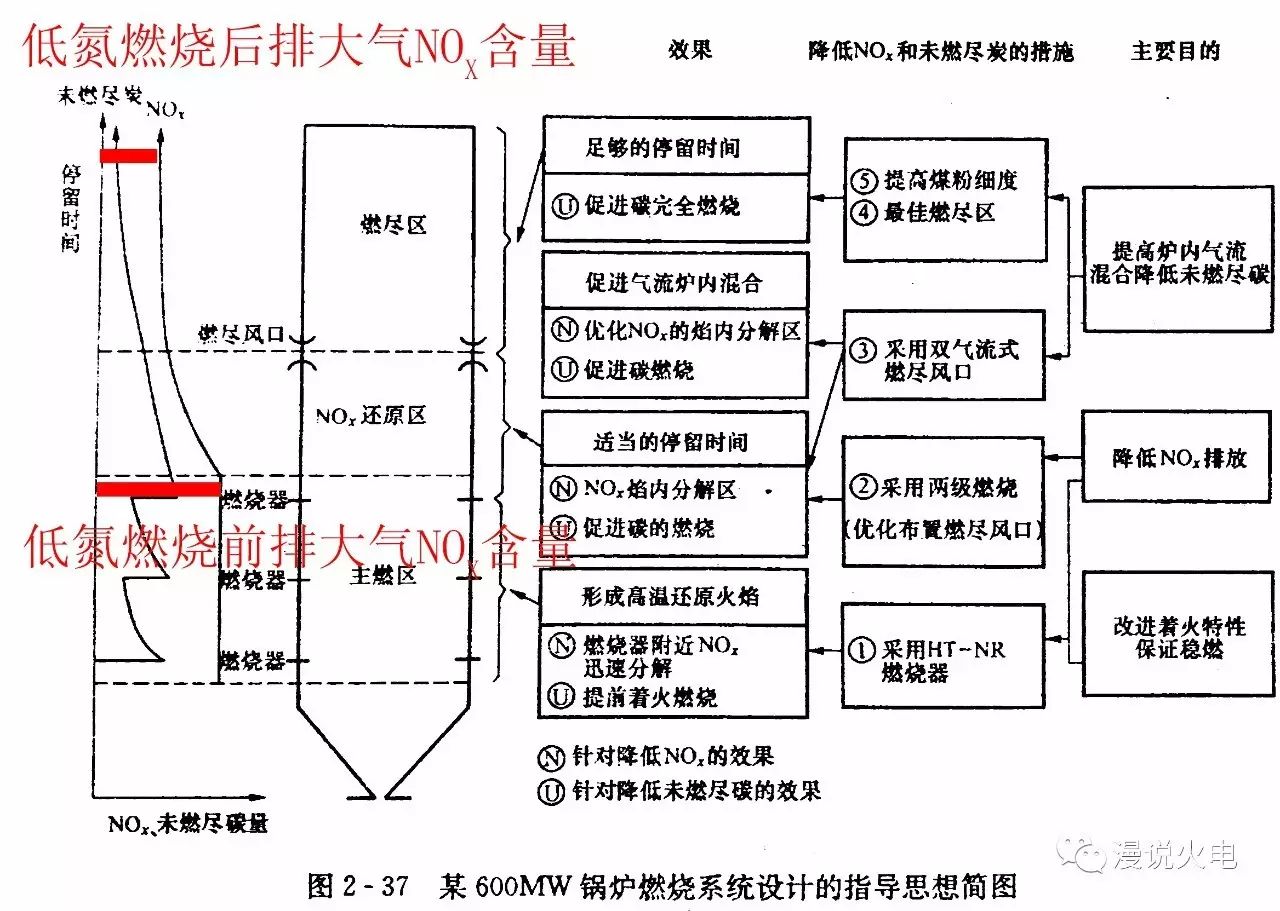
这样是不是就结束了?
显然不是
根据《火电厂大气污染物排放标准(GB 13223-2011 )》
氮氧化物 (以NO2计)排放应当低于100mg/m3
采用W型火焰炉膛的火力发电锅炉,现有循环流化床火力发电锅炉,以及2003年12月31日前建成投产或通过建设项目环境影响报告书审批的火力发电锅炉氮氧化物(以NO2计)排放应当低于200mg/m3
看样子我该说下燃烧器布置方式了
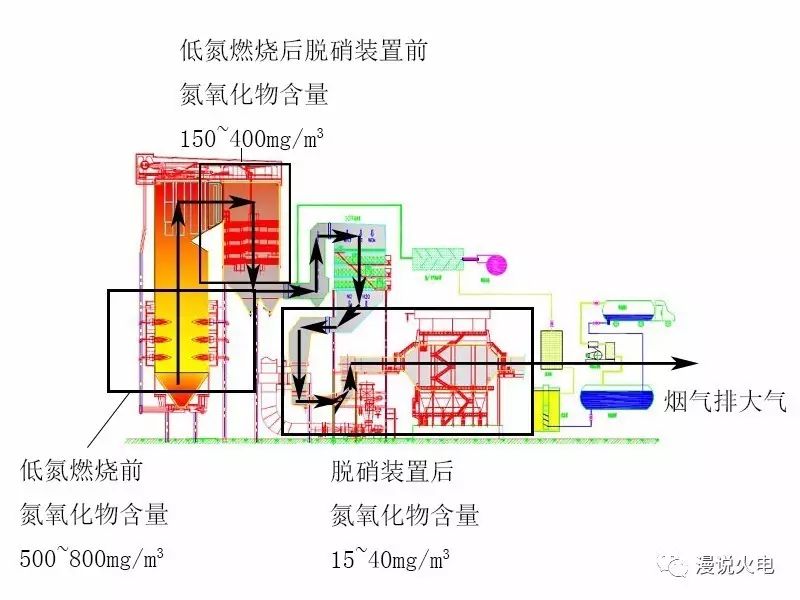
在改造前,锅炉的氮氧化物排放大概在500~800mg/m3,改造后大概在150~400mg/m3,但是这样还达不到国家的排放标准。
于是我们还有第二样法宝,脱硝装置。
问:把氮氧化物变成氮气需要几步?
答:两步
NO+NO2+2NH3=2N2+3H2O
4NO+4NH3+O2=4N2+6H2O

你没看错,真的只有两步。
根据反应条件的不同分为选择性催化还原技术SCR(Selective Catalytic Reduction)和选择性非催化还原技术SNCR(Selective Non-CatalyticReduction)
其实就是有没有催化剂的区别
在没有催化剂的情况下,上述化学反应只是在很窄的温度范围内(980℃左右)进行,采用催化剂时其反应温度可控制在310-420℃下进行,相当于锅炉省煤器与空气预热器之间的烟气温度,上述反应为放热反应,由于NOx在烟气中的浓度较低, 故反应引起催化剂温度的升高可以忽略。
SNCR脱硝效果较差,效率只有30%~70%
SCR脱硝效果较好,效率能达到90%
既然原理这么简单,我们来看下原理图吧。↓↓↓↓
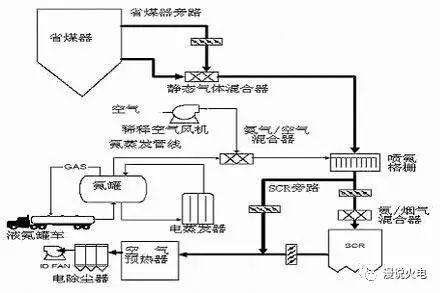
液氨制备氨气
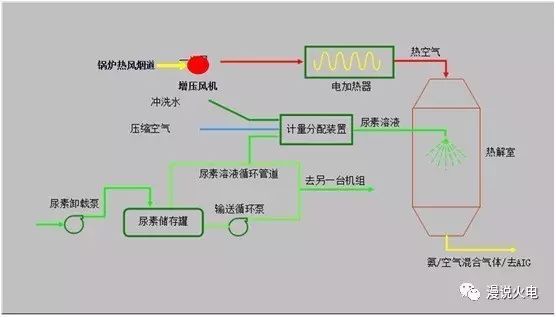
尿素制备氨气

说好的只有两步反应呢?

别打了别打了我知道错了!
因为氨气体积太大,而且不是很安全...我们来百度一下氨气的性质。
氨气,Ammonia, NH3,无色气体。有强烈的刺激气味。密度 0.7710。相对密度0.5971(空气=1.00)。易被液化成无色的液体。在常温下加压即可使其液化(临界温度132.4℃,临界压力11.2兆帕,即112.2大气压)。沸点-33.5℃。也易被固化成雪状固体。熔点-77.75℃。溶于水、乙醇和乙醚。在高温时会分解成氮气和氢气,有还原作用。有催化剂存在时可被氧化成一氧化氮。用于制液氮、氨水、硝酸、铵盐和胺类等。可由氮和氢直接合成而制得,能灼伤皮肤、眼睛、呼吸器官的粘膜,人吸入过多,能引起肺肿胀,以至死亡。

吓得我抱起了我的小鲸鱼
所以在工业上一般不直接运输氨气,而是以氨气被压缩成液体液氨的形式进行运输,但是液氨本身也是重大危险源,为了安全起见,现在用的多是尿素制备氨气,尿素是固体啊亲。它易保存,使用方便,对土壤的破坏作用小,是目前使用量较大的一种化学氮肥。
刚刚整个原理图其实都在把尿素或者液氨制备成氨气。
我们重新来看一下。
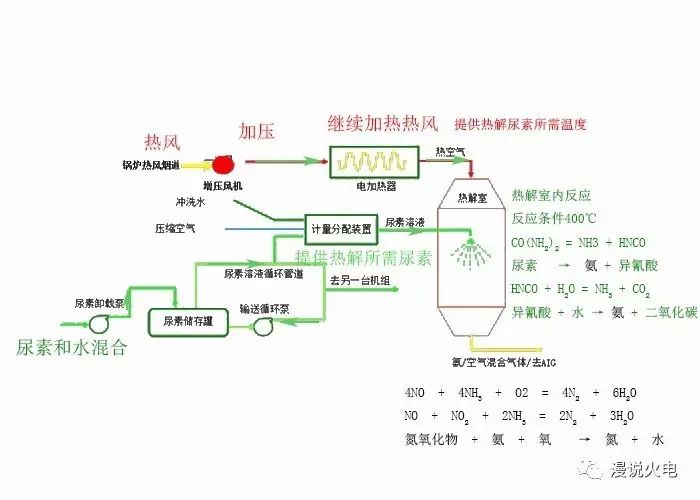
再联系其锅炉总貌来看
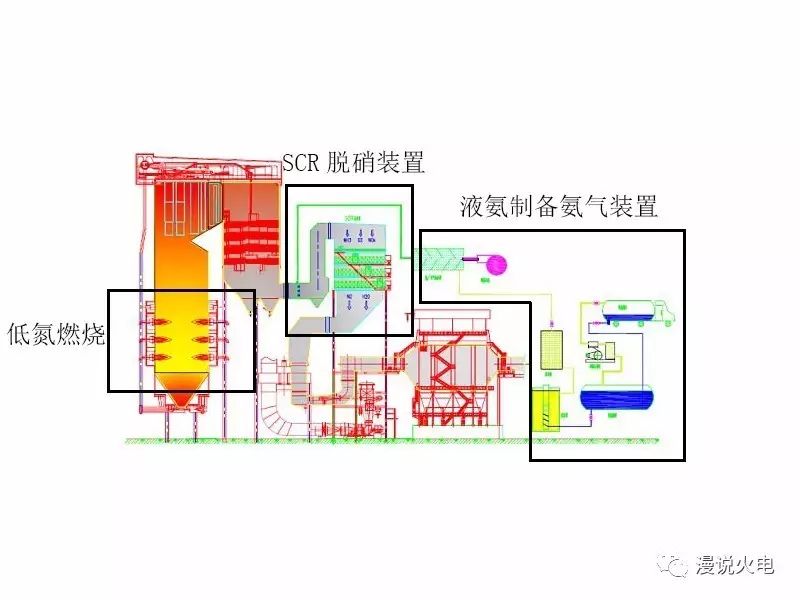
没找到含尿素热解的总貌,用液氨的代替下,一样的。
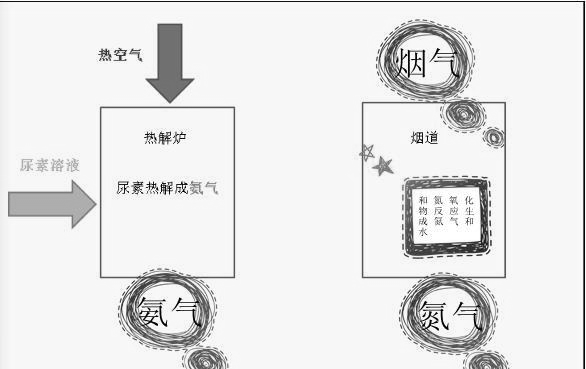
因为热解氨气和氨气还原氮氧化物两步都是有反应条件的,实际在运行中有许多热控保护的要求,具体的运行方式,我们以后再说。
这样一套下来,低氮燃烧+选择催化还原反应,能把锅炉出口的氮氧化物浓度控制在15~40mg/m3左右。相比有所动作之前的500~800mg/m3,可以说几乎是近零排放了。
为了这个近零排放,低氮改造加脱硝装置让火电从业人员经历了灰渣含碳量升高,蒸汽温度异常,汽温壁温偏差大,负荷响应速度变慢,炉内结渣,水冷壁高温腐蚀,空预器堵塞,送引风机失速等等一系列问题。但也熬过来了,算是为了祖国的环保事业出了一份力。
当然主要原因还是因为上了脱硝系统有脱硝上网电价,有钱能使鬼推磨。
但是呢一般一台1000MW的锅炉一台引风机每小时的最大引风量大概在2830000m³/h
一台锅炉一般两台引风机,电厂一般至少两台1000MW的锅炉。也就是说,2000MW的火电厂,如果在迎峰度夏满负荷的情况下,每小时的排风量大概是1132万m³。按30mg/m³的氮氧化物排放量,就是每小时排放339KG的氮氧化物。如果考虑到当地环境的最大承载力,这还是一个不小的数字。但相比原来成吨的排放量已经是很小了。大家可以用700 mg/m³的排放量自己算一下。
我相信有人对这个结果还是不满意。当然这应该也并非我们所能做的极限。




